医药日报 | 百济神州PD-1新适应症有望在近期获批
百济神州「替雷利珠单抗」新适应症有望近期获批,二或三线 NSCLC
12 月 28 日,NMPA 官网显示,百济神州 PD-1 单抗新适应症上市申请已经进入「在审批」阶段,有望在近日获批,用于治疗接受铂类化疗后出现疾病进展的二或三线局部晚期或转移性非小细胞肺癌(NSCLC)。
此项 sBLA 是基于 RATIONALE 303 的中期分析结果,百济神州于去年 11 月宣布该项临床达到 OS 主要终点。
国内第7款!君实生物申报Claudin18.2 ADC
12月28日,CDE官网显示,君实生物注射用JS107临床申请获NMPA受理,JS107是由君实自主研发的注射用重组人源化抗 Claudin18.2 单克隆抗体- MMAE偶联剂,是靶向肿瘤相关蛋白Claudin18.2的抗体偶联药物(ADCs),拟用于治疗胃癌和胰腺癌等晚期恶性肿瘤。
此前,君实自主研发的重组人源化抗Claudin18.2单克隆抗体JS012注射液 已于2021年11月获得国家药监局批准开展临床试验。
诺华斥资15亿美元,扩展眼科疾病基因疗法管线
近日,诺华(Novartis)宣布达成协议,将收购总部位于英国的眼部基因治疗公司Gyroscope Therapeutics的全部剩余股份。

诺华将通过此次收购获得在研一次性基因疗法GT005,该疗法正在进行2期临床试验,用于治疗地理萎缩症(geographic atrophy,GA)。
根据协议内容,诺华将支付8亿美元的预付款,和高达7亿美元的潜在额外里程碑付款。
FDA发布召回通知,原因在「瓶」不在「药」
近日,针对一款硝酸甘油舌喷剂,FDA发布了一则召回消息。因为配药装置故障,可能导致喷剂单次剂量不符合预期,继而发起召回。

一般在我们潜意识里,药品质量影响是指药品制剂本身,往往忽略了包装制型。其实,并非如此,因「包装或装置问题」发起召回的并非个例。2021年11月19日,美国一款消毒剂因瓶子像饮料瓶,可能会导致误服而发起召回。
2021国内药物研发失败案例一览
药物创新研发向来具有「三高一长」的特点,即高投入、高回报、高风险和长周期。
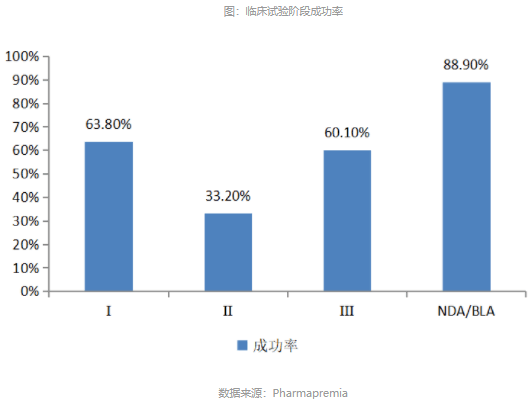
根据Pharmapremia基于近一万项临床试验的统计数据,Ⅰ、Ⅱ、Ⅲ期临床研究的成功率分别是63.8%、33.2%和60.1%。其中Ⅱ期临床失败率最高,成功率仅33.2%。即便通过了Ⅱ期临床试验,Ⅲ期临床试验的成功率也仅为60.1%。
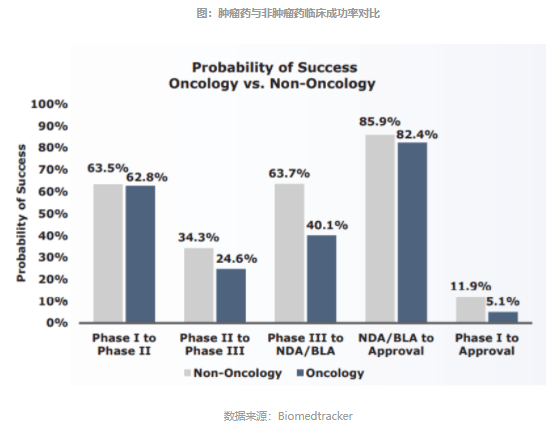
肿瘤药的研发成功率远低于非肿瘤药物的临床成功率。根据Biomedtracker数据库2016年的统计,肿瘤药从Ⅰ期到上市的研发成功率仅为5.1%,不足非肿瘤药的一半。
2021年是我国创新药的丰收之年,同时也有不少明星创新药「壮士断腕」,如百奥泰旗下ADC药物BAT8001终止III期临床试验、泽璟制药的甲苯磺酸多纳非尼片Ⅲ期试验未达预设的优效目标、人福医药1类新药RF-A089胶囊主动终止I期临床试验、信立泰拟终止与VIRACTA的Nanatinostat在中国大陆的独家许可使用权。
编辑/elisa
风险提示:上文所示之作者或者嘉宾的观点,都有其特定立场,投资决策需建立在独立思考之上。富途将竭力但却不能保证以上内容之准确和可靠,亦不会承担因任何不准确或遗漏而引起的任何损失或损害。
