医药日报 | 腾盛博药新冠联合疗法III期临床数据积极
默沙东15价肺炎球菌疫苗获优先审评资格
近日,默沙东公司宣布,美国FDA已授予15价肺炎球菌结合疫苗Vaxneuvance的补充生物制品许可申请(sBLA)优先审评资格,用于帮助6周至17岁儿童预防侵袭性肺炎球菌导致的疾病。

肺炎球菌疾病是由肺炎链球菌感染引起的疾病,对儿童的影响与成人不同,2岁以下儿童特别容易感染肺炎球菌。某些肺炎球菌血清型对儿童危害更大,包括血清型22F、33F和3,占5岁以下儿童所有侵袭性肺炎球菌疾病病例的四分之一以上。
贝达药业再次向港交所递交招股书
近日,贝达药业股份有限公司Betta Pharmaceuticals Co., Ltd向港交所递交招股书,拟在香港主板挂牌上市。这是继其于2021年2月8日递表、2021年5月30日通过上市聆讯失效之后的再一次递表。

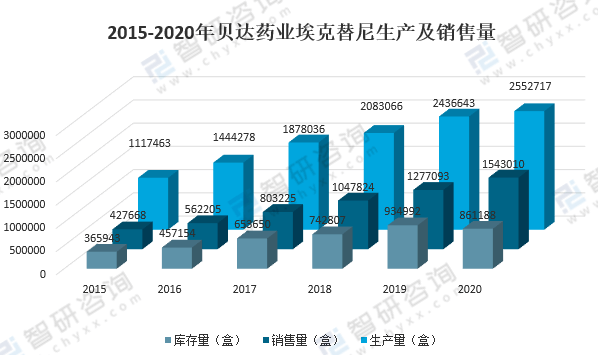
贝达药业于2016年11月7日在深交所挂牌上市。公司首款上市药物埃克替尼(凯美纳?)是中国国内首款自主研发的1类(前称1.1类)小分子靶向抗癌创新药,同时也是我们国内第一个年销售额超过10亿元自主创新药。
FDA扩大君实生物的新冠药物治疗人群范围
12月15日,公司宣布FDA扩大埃特司韦单抗及巴尼韦单抗双抗体疗法紧急使用授权范围至12岁以下人群。
截至目前,双抗体疗法是全球首个且唯一获紧急使用授权覆盖12岁以下人群的中和抗体疗法,可为全年龄段的高风险人群提供治疗和预防COVID-19的选择。

CDE正式发布3份基因治疗相关指导原则
12月3日,国家药监局药审中心发布《基因治疗产品非临床研究与评价技术指导原则(试行)》《基因修饰细胞治疗产品非临床研究技术指导原则(试行)》《基因治疗产品长期随访临床研究技术指导原则(试行)》,指导规范国内基因治疗产品非临床研究与评价和基因治疗类药物临床试验。
3个指导原则均自发布之日起施行。值得注意的是,尽管基因疗法在治愈疾病方面具有极大潜力,但它也会对人体带来长期或永久性影响,所以非常有必要对参加基因治疗临床试验的受试者开展长期随访。
腾盛博药-B新冠联合疗法使住院及死亡复合终点降低80%
12月5日,公司发布公告称,该公司已收到由美国国立卫生研究院支持的ACTIV-2三期临床试验分析、基于患者总人数的关键性数据分析结果。

结果显示,公司在研的新型冠状病毒联合疗法(即安巴韦单抗/罗米司韦单抗联合疗法,在疾病进展高风险的门诊患者中,住院及死亡的复合终点降低80%,治疗组受试者在28天治疗期内无死亡,而安慰剂组有9例死亡。
华润三九董事长辞职
12月3日,华润三九发布公告称,董事会收到董事长王春城提交的辞职报告,由于工作变动原因,王春城提请辞去董事长、董事职务,辞职后不再在华润三九担任职务。

除董事长王春城外,华润三九9月10日还发布公告称,董事郭巍、邓荣辉以及副总裁谈英宣布辞职。
编辑/elisa
风险提示:上文所示之作者或者嘉宾的观点,都有其特定立场,投资决策需建立在独立思考之上。富途将竭力但却不能保证以上内容之准确和可靠,亦不会承担因任何不准确或遗漏而引起的任何损失或损害。
